Desactivando RpoS: el regulador que controla la adaptación y virulencia en Pseudomonas aeruginosa
AUTORES
Luis Mauricio Salazar-Garcia 1, Jose Manuel Villalobos-Escobedo 2
Industrial Genomics Laboratory, FEMSA Biotechnology Center, School of Engineering and Sciences, Tecnológico de Monterrey, Monterrey, Nuevo Leon, Mexico.1
Integrative Biology Research Unit, The Institute for Obesity Research, Tecnológico de Monterrey, Monterrey, Nuevo Leon, Mexico.2
e-mail: jose.villalobos@tec.mx
Descarga el artículo
Un vistazo al gen maestro del estrés bacteriano
En este estudio se descifró cómo la bacteria Pseudomonas aeruginosa —uno de los patógenos oportunistas más persistentes del mundo— reorganiza su expresión génica cuando pierde su regulador maestro: el factor sigma RpoS (σ^S).
Mediante edición genética por CRISPR/Cas9, se generó un mutante de la cepa virulenta PA14 donde se introdujo un codón STOP en el gen rpoS, desactivando por completo su función. Esta modificación permitió observar cómo la bacteria responde molecularmente cuando su sistema de defensa ante el estrés queda fuera de servicio.
La pérdida de RpoS provoca una reprogramación masiva del transcriptoma, alterando rutas metabólicas que sostienen la resistencia y la capacidad infecciosa de la bacteria.
El factor sigma RpoS no solo regula la supervivencia bajo condiciones adversas como la falta de nutrientes o el estrés oxidativo, sino que también influye en la expresión de genes de virulencia.
Este estudio ofrece una visión detallada del regulón RpoS en la cepa PA14, más virulenta que otras variantes como PAO1, y contribuye a comprender los mecanismos que hacen de P. aeruginosa un microorganismo tan exitoso en ambientes clínicos e industriales.
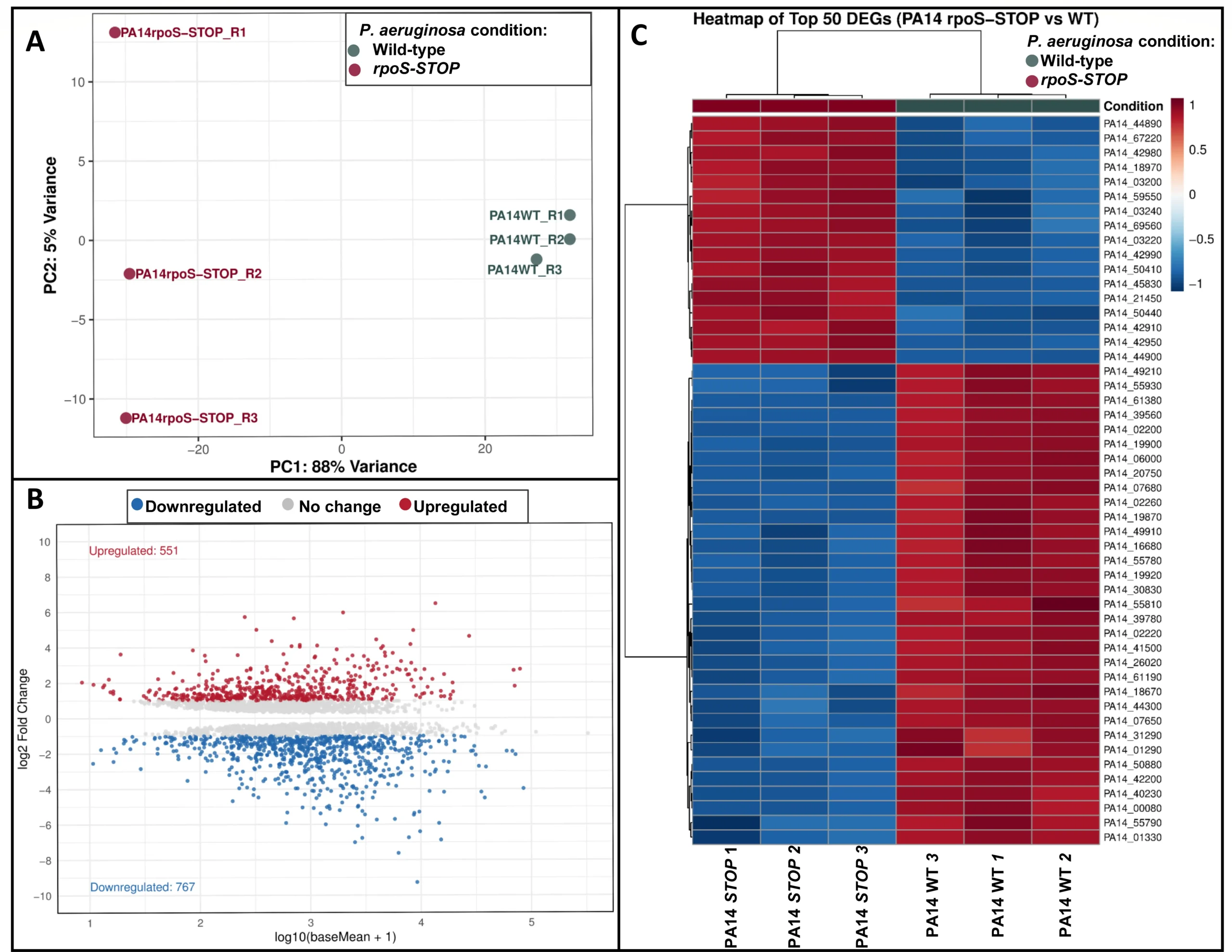
Fig 1: Análisis transcriptómico de cepas de tipo salvaje PA14 de P. aeruginosa y cepas mutantes rpoS-STOP .
- Lyczak JB, Cannon CL, Pier GB. 2000. Establishment of Pseudomonas aeruginosa infection: lessons from a versatile opportunist. Microbes Infect 2:1051–1060.
- Estahbanati HK, Kashani PP, Ghanaatpisheh F. 2002. Frequency of Pseudomonas aeruginosa serotypes in burn wound infections and their resistance to antibiotics. Burns 28:340–348.
- Sadikot RT, Blackwell TS, Christman JW, Prince AS. 2005. Pathogen–host interactions in Pseudomonas aeruginosa pneumonia. Am J Respir Crit Care Med 171:1209–1223.
- Diggle SP, Whiteley M. 2020. Microbe Profile: Pseudomonas aeruginosa: opportunistic pathogen and lab rat. Microbiology (Reading) 166:30–33.
- Denissen J, Reyneke B, Waso-Reyneke M, Havenga B, Barnard T, Khan S, Khan W. 2022. Prevalence of ESKAPE pathogens in the environment: antibiotic resistance status, community-acquired infection and risk to human health. Int J Hyg Environ Health 244:114006.
- Lee DG, Urbach JM, Wu G, Liberati NT, Feinbaum RL, Miyata S, Diggins LT, He J, Saucier M, Déziel E, Friedman L, Li L, Grills G, Montgomery K, Kucherlapati R, Rahme LG, Ausubel FM. 2006. Genomic analysis reveals that Pseudomonas aeruginosa virulence is combinatorial. Genome Biol 7:1–14.
- Wolfgang MC, Kulasekara BR, Liang X, Boyd D, Wu K, Yang Q, Miyada CG, Lory S. 2003. Conservation of genome content and virulence determinants among clinical and environmental isolates of Pseudomonas aeruginosa. Proc Natl Acad Sci USA 100:8484–8489.
- Suh SJ, Silo-Suh L, Woods DE, Hassett DJ, West SE, Ohman DE. 1999. Effect of rpoS mutation on the stress response and expression of virulence factors in Pseudomonas aeruginosa. J Bacteriol 181:3890–3897.
- Whiteley M, Parsek MR, Greenberg EP. 2000. Regulation of quorum sensing by RpoS in Pseudomonas aeruginosa. J Bacteriol 182:4356–4360.
- Schuster M, Lostroh CP, Ogi T, Greenberg EP. 2003. Identification, timing, and signal specificity of Pseudomonas aeruginosa quorum-controlled genes: a transcriptome analysis. J Bacteriol 185:2066–2079.
- Muriel-Millán LF, Montelongo-Martínez LF, González-Valdez A, Bedoya-Pérez LP, Cocotl-Yañez M, Soberón-Chávez G. 2024. The alternative sigma factor RpoS regulates Pseudomonas aeruginosa quorum sensing response by repressing the pqsABCDE operon and activating vfr. Mol Microbiol 121:291–303.
- Mathee K, Narasimhan G, Valdes C, Qiu X, Matewish JM, Koehrsen M, Rokas A, Yandava CN, Engels R, Zeng E, Olavarietta R, Doud M, Smith RS, Montgomery P, White JR, Godfrey PA, Kodira C, Birren B, Galagan JE, Lory S. 2008. Dynamics of Pseudomonas aeruginosa genome evolution. Proc Natl Acad Sci USA 105:3100–3105.
- Freschi L, Vincent AT, Jeukens J, Emond-Rheault J-G, Kukavica-Ibrulj I, Dupont M-J, Charette SJ, Boyle B, Levesque RC. 2019. The Pseudomonas aeruginosa pan-genome provides new insights on its population structure, horizontal gene transfer, and pathogenicity. Genome Biol Evol 11:109–120.
- Volke DC, Martino RA, Kozaeva E, Smania AM, Nikel PI. 2022. Modular (de)construction of complex bacterial phenotypes by CRISPR/nCas9-assisted, multiplex cytidine base-editing. Nat Commun 13:3026.
- Chen S, Zhou Y, Chen Y, Gu J. 2018. Fastp: an ultra-fast all-in-one FASTQ preprocessor. Bioinformatics 34:i884–i890.
- Kim D, Paggi JM, Park C, Bennett C, Salzberg SL. 2019. Graph-based genome alignment and genotyping with HISAT2 and HISAT-genotype. Nat Biotechnol 37:907–915.
- Liao Y, Smyth GK, Shi W. 2014. featureCounts: an efficient general purpose program for assigning sequence reads to genomic features. Bioinformatics 30:923–930.
- Love MI, Huber W, Anders S. 2014. Moderated estimation of fold change and dispersion for RNA-seq data with DESeq2. Genome Biol 15:550.



