Genómica y metabolómica de Trichoderma harzianum T9: un hongo del desierto con potencial para la agricultura sostenible
AUTORES
Francisco Vargas-Gasca1, Enrique Pola-Sánchez2, Ana Valeria García-Lartigue2, Alan D. Gomez-Vargas3, Pablo Cruz-Morales4, Ana Calheiros Carvalho4, Daniela Rago4, Linda Ahonen4, Elva Teresa Aréchiga-Carvajal5, José Manuel Villalobos-Escobedo2, Vianey Olmedo-Monfil1
Universidad de Guanajuato.1
Institute for Obesity Research.2
CINVESTAV Irapuato.3
Technical University of Denmark.4
Universidad Autónoma de Nuevo León.5
e-mail: jose.villalobos@tec.mx
Descarga el artículo completo
El uso de microorganismos como alternativa a los pesticidas químicos se ha convertido en una prioridad para lograr una agricultura más sostenible.
Frente a los retos del cambio climático y el desgaste del suelo agrícola, desciframos el genoma de Trichoderma harzianum T9 —una cepa aislada de los suelos áridos de Mina, Nuevo León— capaz de sobrevivir donde casi nada crece.
Este hongo del desierto no solo resiste temperaturas extremas y suelos alcalinos: también inhibe con alta eficacia a patógenos devastadores como Macrophomina spp. y Neopestalotiopsis rosae, responsables de pérdidas millonarias en los cultivos de fresa de México.
El genoma de T. harzianum T9 representa un avance hacia una agricultura más resiliente y sostenible: una biotecnología que surge del desierto mexicano para transformar la manera en que protegemos nuestros cultivos.

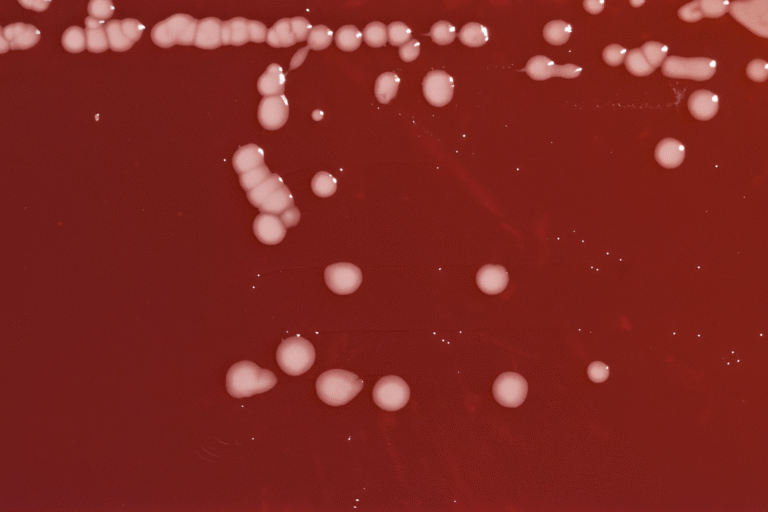
A) Vista superior y (B) vista inferior de las placas que muestran las interacciones entre los fitopatógenos Macrophomina sp. (M.sp), N. rosae (N.r), Fusarium sp. (F.sp) y Fusarium UG (F.UG) con las cepas de Trichoderma T. harzianum T9, T. harzianum M10 y T. atroviride IMI206040 (T.a). Los fitopatógenos se colocaron en el lado derecho, mientras que las cepas de Trichoderma se ubicaron en el lado izquierdo de la placa. Las fotografías fueron tomadas después de 96 horas de interacción.
C) Acercamiento de la zona de interacción entre M.sp o N.r con las cepas de Trichoderma T9 y M10.
D) Área promedio de las colonias de M.sp y (E) N.r en interacción con diferentes cepas de Trichoderma. El control representa el tamaño promedio de las colonias de cada patógeno creciendo de forma individual.
Los asteriscos indican diferencias estadísticas según la prueba Tukey-HSD con un nivel de significancia de α < 0.05, con p < 0.05. n = 3.

A) Vista superior de placas que muestran las interacciones entre T. harzianum T9, T. harzianum M10 y T. atroviride IMI206040 (T.a) con Macrophomina sp. (M.sp) o (C) N. rosae (N.r), cultivadas en medio PDA a pH 8.5. Los fitopatógenos se muestran en el lado derecho, mientras que las cepas de Trichoderma están en el lado izquierdo. Las fotografías fueron tomadas después de 96 horas de interacción.
B) Área promedio de las colonias de M.sp y (D) N.r en interacción con diferentes cepas de Trichoderma. El control representa el tamaño promedio de las colonias de cada patógeno creciendo de forma individual.
Los asteriscos indican diferencias estadísticas según la prueba Tukey-HSD con un nivel de significancia de α < 0.05, con p < 0.05. n = 3.

A) Análisis de espectros de k-mers utilizando Jellyfish con k = 21 para el conteo de k-mers, y GenomeScope 1.0 para el ajuste de modelos que estiman el tamaño del genoma, heterocigosidad y repetitividad.
B) Evaluación de la completitud del ensamblaje mediante el programa BUSCO (Benchmarking Universal Single-Copy Orthologs) utilizando el conjunto de datos de hongos.
C) Predicción y cuantificación de las regiones de baja complejidad y de los elementos repetitivos presentes en el genoma.

A) Tabla con las estadísticas de la anotación genómica.
B) Completitud de la anotación evaluada mediante BUSCO (Benchmarking Universal Single-Copy Orthologs) utilizando el conjunto de datos de hongos, basada en los transcritos extraídos con GFFread.
C) Distribución de la longitud de los genes.

A) Árbol filogenético enraizado de 30 especies fúngicas, generado mediante OrthoVenn3 y ROADIES. Fusarium oxysporum y Fusarium graminearum se utilizaron como especies externas (outgroups) en el análisis.
B) Diagrama de Venn que muestra las familias de clústeres ortólogos únicas y compartidas entre cinco especies de Trichoderma, incluida la cepa secuenciada T. harzianum T9, generado con OrthoVenn3.

A) Diagrama de caja (boxplot) que muestra el porcentaje de SNPs en los genes ortólogos de T9 comparados con las cepas T. harzianum Th6, M10, T22, Th0179, Th3844 y TR274, utilizando T. atroviride IMI206040 como control.
B) Diagrama de dispersión (scatterplot) que muestra el número de SNPs a lo largo de los genes ortólogos en la comparación entre T9 y la cepa M10.
C) Anotación de los genes con los porcentajes más altos de SNPs (>11%) en la comparación de T9 frente a M10.

Esta predicción se realizó utilizando fungiSMASH (la versión para análisis fúngicos de AntiSMASH).
Se identificaron diez familias de clústeres, siendo T1PKS, NRPS y terpenos las tres más abundantes.

A) Cromatogramas de iones extraídos de (aquí deben añadirse los valores m/z de cada cromatograma extraído).
B) Espectros de fragmentación del ion precursor con m/z = 1175.7762 [M+H]+, correspondiente al peptaíbolo de 11 aminoácidos.
C) Espectros de fragmentación del ion precursor con m/z = 1189.7918 [M+H]+, correspondiente al peptaíbolo de 11 aminoácidos.
D) Espectros de fragmentación del ion precursor con m/z = 1442.9344 [M+H]+, correspondiente al peptaíbolo de 14 aminoácidos.

A) Reconstrucción filogenética con CORASON usando “gene-name” como gen de consulta y el clúster NRPS de T. harzianum responsable de peptaíbolos de 11 y 14 residuos. Los genes ausentes en el clúster de referencia se resaltan y se codifican por color con base en el análisis BLAST.
B) Vía biosintética de los peptaíbolos de 12 y 14 residuos. Los residuos omitidos durante el proceso de biosíntesis, debido a la funcionalidad de la NRPS, se muestran en azul.
- Sariah, M., Choo, C. W., Zakaria, H. & Norihan, M. S. Quantification and characterisation of Trichoderma spp. from different ecosystems. Mycopathologia 159, 113–117 (2005).
- Woo, S. L., Hermosa, R., Lorito, M. & Monte, E. Trichoderma: a multipurpose, plant-beneficial microorganism for eco-sustainable agriculture. Nat. Rev. Microbiol. 21, 312–326 (2023).
- Guzmán-Guzmán, P., Porras-Troncoso, M. D., Olmedo-Monfil, V. & Herrera-Estrella, A. Trichoderma species: versatile plant symbionts. Phytopathology 109, 6–16 (2019).
- Tyśkiewicz, R., Nowak, A., Ozimek, E. & Jaroszuk-Ściseł, J. Trichoderma: the current status of its application in agriculture for the biocontrol of fungal phytopathogens and stimulation of plant growth. Int. J. Mol. Sci. 23, 2329 (2022).
- Yao, X., Guo, H., Zhang, K., Zhao, M., Ruan, J. & Chen, J. Trichoderma and its role in biological control of plant fungal and nematode disease. Front. Microbiol. 14, 1160551 (2023).
- Guo, R., Wang, Z., Huang, Y., Fan, H. & Liu, Z. Biocontrol potential of saline- or alkaline-tolerant Trichoderma asperellum mutants against three pathogenic fungi under saline or alkaline stress conditions. Braz. J. Microbiol. 49, 236–245 (2018).
- Bueno de Mesquita, C. P. et al. Microbial ecology and site characteristics underlie differences in salinity–methane relationships in coastal wetlands. J. Geophys. Res. Biogeosci. 129, e2024JG008133 (2024).
- Cabral-Miramontes, J. P., Olmedo-Monfil, V., Lara-Banda, M., Zúñiga-Romo, E. R. & Aréchiga-Carvajal, E. T. Promotion of plant growth in arid zones by selected Trichoderma spp. strains with adaptation plasticity to alkaline pH. Biology (Basel) 11, 1206 (2022). https://doi.org/10.3390/biology11081206
- Enriquez-Felix, E. E. et al. Argonaute and Dicer are essential for communication between Trichoderma atroviride and fungal hosts during mycoparasitism. Microbiol. Spectr. 12, e0316523 (2024). https://doi.org/10.1128/spectrum.03165-23
- Özkale, E., Yörük, E., Budak, M. & Korkmaz, E. M. Trichoderma atroviride suppresses Fusarium graminearum by altering primary and secondary metabolite biosynthesis profiling. Plant Pathol. 72, 1428–1441 (2023).
- Rebollar-Alviter, A., Silva-Rojas, H. V., Fuentes-Aragón, D., Acosta-González, U., Martínez-Ruiz, M. & Parra-Robles, B. E. An emerging strawberry fungal disease associated with root rot, crown rot and leaf spot caused by Neopestalotiopsis rosae in Mexico. Plant Dis. 104, 2054–2059 (2020).
- Chaverri, P., Branco-Rocha, F., Jaklitsch, W., Gazis, R., Degenkolb, T. & Samuels, G. J. Systematics of the Trichoderma harzianum species complex and the re-identification of commercial biocontrol strains. Mycologia 107, 558–590 (2015).
- Al-Salihi, S. A. & Alberti, F. Genomic based analysis of the biocontrol species Trichoderma harzianum: a model resource of structurally diverse pharmaceuticals and biopesticides. J. Fungi 9, 895 (2023).
- Sambrook, J. & Russell, D. W. Purification of nucleic acids by extraction with phenol: chloroform. Cold Spring Harb. Protoc. 2006, pdb-prot4455 (2006).
- White, T. J., Bruns, T., Lee, S. J. W. T. & Taylor, J. Amplification and direct sequencing of fungal ribosomal RNA genes for phylogenetics. In PCR Protocols: A Guide to Methods and Applications 315–322 (Academic Press, 1990).
- Swift, M. L. GraphPad Prism, data analysis, and scientific graphing. J. Chem. Inf. Comput. Sci. 37, 411–412 (1997).
- Andrews, S. FastQC: a quality control tool for high throughput sequence data. Babraham Bioinformatics http://www.bioinformatics.babraham.ac.uk/projects/fastqc (2010).
- Bolger, A. M., Lohse, M. & Usadel, B. Trimmomatic: a flexible trimmer for Illumina sequence data. Bioinformatics 30, 2114–2120 (2014).
- Bankevich, A. et al. SPAdes: a new genome assembly algorithm and its applications to single-cell sequencing. J. Comput. Biol. 19, 455–477 (2012).
- Astashyn, A. et al. Rapid and sensitive detection of genome contamination at scale with FCS-GX. Genome Biol. 25, 60 (2024). https://doi.org/10.1186/s13059-024-03198-7
- Gurevich, A., Saveliev, V., Vyahhi, N. & Tesler, G. QUAST: quality assessment tool for genome assemblies. Bioinformatics 29, 1072–1075 (2013). https://doi.org/10.1093/bioinformatics/btt086
- Simão, F. A., Waterhouse, R. M., Ioannidis, P., Kriventseva, E. V. & Zdobnov, E. M. BUSCO: assessing genome assembly and annotation completeness with single-copy orthologs. Bioinformatics 31, 3210–3212 (2015).
- Baril, T., Galbraith, J. G. & Hayward, A. Earl Grey: a fully automated user-friendly transposable element annotation and analysis pipeline. Mol. Biol. Evol. 41, msae068 (2024). https://doi.org/10.1093/molbev/msae068
- Hubley, R. et al. The Dfam database of repetitive DNA families. Nucleic Acids Res. 44, D81–D89 (2016).
- Bruna, T., Hoff, K. J., Lomsadze, A., Stanke, M. & Borodovsky, M. BRAKER2: automatic eukaryotic genome annotation with GeneMark-EP+ and AUGUSTUS supported by a protein database. NAR Genom. Bioinform. 3, lqaa108 (2021). https://doi.org/10.1093/nargab/lqaa108
- Kuznetsov, D. et al. OrthoDB v11: annotation of orthologs in the widest sampling of organismal diversity. Nucleic Acids Res. 51, D445–D451 (2023). https://doi.org/10.1093/nar/gkac998
- Tang, H. et al. JCVI: a versatile toolkit for comparative genomics analysis. Imeta 3, e211 (2024).
- Huerta-Cepas, J., Forslund, K., Coelho, L. P., Szklarczyk, D., Jensen, L. J., von Mering, C. & Bork, P. Fast genome-wide functional annotation through orthology assignment by eggNOG-Mapper. Mol. Biol. Evol. 34, 2115–2122 (2017). https://doi.org/10.1093/molbev/msx148
- Jones, P. et al. InterProScan 5: genome-scale protein function classification. Bioinformatics 30, 1236–1240 (2014). https://doi.org/10.1093/bioinformatics/btu031
- Zheng, J., Ge, Q., Yan, Y., Zhang, X., Huang, L. & Yin, Y. dbCAN3: automated carbohydrate-active enzyme and substrate annotation. Nucleic Acids Res. 51, W115–W121 (2023).
- Cuomo, C. A. et al. The Fusarium graminearum genome reveals a link between localized polymorphism and pathogen specialization. Science 317, 1400–1402 (2007). https://doi.org/10.1126/science.1143708
- Ma, L. J. et al. Comparative genomics reveals mobile pathogenicity chromosomes in Fusarium. Nature 464, 367–373 (2010). https://doi.org/10.1038/nature08850
- He, Y. & Zhu, H. Whole genome sequencing and analysis of the weed pathogen Trichoderma polysporum HZ-31. Sci. Rep. 14, 15228 (2024). https://doi.org/10.1038/s41598-024-66041-w
- Studholme, D. J. et al. Investigating the beneficial traits of Trichoderma hamatum GD12 for sustainable agriculture—insights from genomics. Front. Plant Sci. 4, 258 (2013). https://doi.org/10.3389/fpls.2013.00258
- Davolos, D. et al. A genomic and transcriptomic study on the DDT-resistant Trichoderma hamatum FBL 587: first genetic data into mycoremediation strategies for DDT-polluted sites. Microorganisms 9, 1680 (2021). https://doi.org/10.3390/microorganisms9081680
- Li, L., Zeng, X., Chen, J., Tian, J., Huang, J. & Su, S. Genome sequence of the fungus Trichoderma asperellum SM-12F1 revealing candidate functions of growth promotion, biocontrol, and bioremediation. PhytoFrontiers 1, 171–173 (2021). https://doi.org/10.1094/PHYTOFR-12-20-0052-A
- Li, W. C. et al. Complete genome sequences and genome-wide characterization of Trichoderma biocontrol agents provide new insights into their evolution and variation in genome organization, sexual development, and fungal–plant interactions. Microbiol. Spectr. 9, e0066321 (2021). https://doi.org/10.1128/Spectrum.00663-21
- Baroncelli, R., Zapparata, A., Piaggeschi, G., Sarrocco, S. & Vannacci, G. Draft whole-genome sequence of Trichoderma gamsii T6085, a promising biocontrol agent of Fusarium head blight on wheat. Genome Announc. 4, e01747-15 (2016). https://doi.org/10.1128/genomeA.01747-15
- Kubicek, C. P. et al. Comparative genome sequence analysis underscores mycoparasitism as the ancestral lifestyle of Trichoderma. Genome Biol. 12, R40 (2011). https://doi.org/10.1186/gb-2011-12-4-r40
- Druzhinina, I. S. et al. Massive lateral transfer of genes encoding plant cell wall-degrading enzymes to the mycoparasitic fungus Trichoderma from its plant-associated hosts. PLoS Genet. 14, e1007322 (2018). https://doi.org/10.1371/journal.pgen.1007322
- Kubicek, C. P. et al. Evolution and comparative genomics of the most common Trichoderma species. BMC Genomics 20, 485 (2019). https://doi.org/10.1186/s12864-019-5680-7
- Steindorff, A. S. et al. Identification of mycoparasitism-related genes against the phytopathogen Sclerotinia sclerotiorum through transcriptome and expression profile analysis in Trichoderma harzianum. BMC Genomics 15, 204 (2014). https://doi.org/10.1186/1471-2164-15-204
- Yang, D. et al. Genome sequence and annotation of Trichoderma parareesei, the ancestor of the cellulase producer Trichoderma reesei. Genome Announc. 3, e00885-15 (2015). https://doi.org/10.1128/genomeA.00885-15
- Li, W. C. et al. Trichoderma reesei complete genome sequence, repeat-induced point mutation, and partitioning of CAZyme gene clusters. Biotechnol. Biofuels 10, 170 (2017). https://doi.org/10.1186/s13068-017-0825-x
- Suazo Tejada, A. K. et al. Genome sequencing and de novo assembly of Trichoderma longibrachiatum isolate collected from Florida agricultural soils. Microbiol. Resour. Announc. 13, e00906-23 (2024). https://doi.org/10.1128/mra.00906-23
- Rosolen, R. R. et al. Whole-genome sequencing and comparative genomic analysis of potential biotechnological strains of Trichoderma harzianum, Trichoderma atroviride, and Trichoderma reesei. Mol. Genet. Genomics 298, 735–754 (2023). https://doi.org/10.1007/s00438-023-02013-5
- Sun, J., Lu, F., Luo, Y., Bie, L., Xu, L. & Wang, Y. OrthoVenn3: an integrated platform for exploring and visualizing orthologous data across genomes. Nucleic Acids Res. 51, W397–W403 (2023).
- Edgar, R. C. MUSCLE: multiple sequence alignment with high accuracy and high throughput. Nucleic Acids Res. 32, 1792–1797 (2004). https://doi.org/10.1093/nar/gkh340
- Capella-Gutiérrez, S., Silla-Martínez, J. M. & Gabaldón, T. trimAl: a tool for automated alignment trimming in large-scale phylogenetic analyses. Bioinformatics 25, 1972–1973 (2009). https://doi.org/10.1093/bioinformatics/btp348
- Price, M. N., Dehal, P. S. & Arkin, A. P. FastTree 2—approximately maximum-likelihood trees for large alignments. PLoS One 5, e9490 (2010).
- Gupta, A., Mirarab, S. & Turakhia, Y. Accurate, scalable, and fully automated inference of species trees from raw genome assemblies using ROADIES. Proc. Natl Acad. Sci. USA 122, e2500553122 (2025). https://doi.org/10.1073/pnas.2500553122
- Li, H. Aligning sequence reads, clone sequences and assembly contigs with BWA-MEM. arXiv (2013). https://doi.org/10.48550/arXiv.1303.3997
- Li, H. et al. The Sequence Alignment/Map format and SAMtools. Bioinformatics 25, 2078–2079 (2009). https://doi.org/10.1093/bioinformatics/btp352
- Danecek, P. et al. The variant call format and VCFtools. Bioinformatics 27, 2156–2158 (2011). https://doi.org/10.1093/bioinformatics/btr330
- Emms, D. M. & Kelly, S. OrthoFinder: phylogenetic orthology inference for comparative genomics. Genome Biol. 20, 238 (2019). https://doi.org/10.1186/s13059-019-1832-y
- Heuckeroth, S. et al. Reproducible mass spectrometry data processing and compound annotation in MZmine 3. Nat. Protoc. 19, 2597–2641 (2024).
- Navarro-Muñoz, J. C. et al. A computational framework to explore large-scale biosynthetic diversity. Nat. Chem. Biol. 16, 60–68 (2020).
- Marçais, G. & Kingsford, C. A fast, lock-free approach for efficient parallel counting of occurrences of k-mers. Bioinformatics 27, 764–770 (2011).
- Vurture, G. W. et al. GenomeScope: fast reference-free genome profiling from short reads. Bioinformatics 33, 2202–2204 (2017).
- Baroncelli, R. et al. Draft whole-genome sequence of the biocontrol agent Trichoderma harzianum T6776. Genome Announc. 3, e00647-15 (2015). https://doi.org/10.1128/genomeA.00647-15
- Fanelli, F., Liuzzi, V. C., Logrieco, A. F. & et al. Genomic characterization of Trichoderma atrobrunneum (T. harzianum species complex) ITEM 908: insight into the genetic endowment of a multi-target biocontrol strain. BMC Genomics 19, 662 (2018). https://doi.org/10.1186/s12864-018-5049-3
- Beijen, E. P. W. & Ohm, R. A. Genome annotations for the ascomycete fungi Trichoderma harzianum, Trichoderma aggressivum and Purpureocillium lilacinum. Microbiol. Resour. Announc. 13, e01153-23 (2024). https://doi.org/10.1128/mra.01153-23
- Pertea, G. & Pertea, M. GFF utilities: GffRead and GffCompare. F1000Research 9, ISCB-Comm (2020).
- Dixon, D. P., Skipsey, M. & Edwards, R. Roles for glutathione transferases in plant secondary metabolism. Phytochemistry 71, 338–350 (2010).
- Baker, S. E., Perrone, G., Richardson, N. M., Gallo, A. & Kubicek, C. P. Phylogenomic analysis of polyketide synthase-encoding genes in Trichoderma. Microbiology 158, 147–154 (2012).
- Bumpus, S. B., Magarvey, N. A., Kelleher, N. L., Walsh, C. T. & Calderone, C. T. Polyunsaturated fatty-acid-like trans-enoyl reductases utilized in polyketide biosynthesis. J. Am. Chem. Soc. 130, 11614–11616 (2008).
- Yao, T., Wang, X. & Chen, F. The role of enoyl reductase in the Monacolin K biosynthesis pathway in Monascus spp. J. Fungi 11, 199 (2025).
- Moummou, H., Kallberg, Y., Tonfack, L. B., Persson, B. & van Der Rest, B. The plant short-chain dehydrogenase (SDR) superfamily: genome-wide inventory and diversification patterns. BMC Plant Biol. 12, 219 (2012).
- Mukherjee, P. K. et al. Two classes of new peptaibols are synthesized by a single non-ribosomal peptide synthetase of Trichoderma virens. J. Biol. Chem. 286, 4544–4554 (2011).
- Nandini, B., Puttaswamy, H., Saini, R. K., Prakash, H. S. & Geetha, N. Trichovariability in rhizosphere soil samples and their biocontrol potential against downy mildew pathogen in pearl millet. Sci. Rep. 11, 9517 (2021). https://doi.org/10.1038/s41598-021-89061-2
- Xue, M. et al. Screening and identification of Trichoderma strains isolated from natural habitats in China with potential agricultural applications. Biomed. Res. Int. 2021, 7913950 (2021). https://doi.org/10.1155/2021/7913950
- Mukherjee, P. K., Mendoza-Mendoza, A., Zeilinger, S. & Horwitz, B. A. Mycoparasitism as a mechanism of Trichoderma-mediated suppression of plant diseases. Fungal Biol. Rev. 38, 15–33 (2022). https://doi.org/10.1016/j.fbr.2021.11.004
- Timmusk, S., Nevo, E., Ayele, F., Noe, S. & Niinemets, Ü. Fighting Fusarium pathogens in the era of climate change: a conceptual approach. Pathogens 9, 419 (2020).
- Singh, N. K., Tralamazza, S. M., Abraham, L. N., Glauser, G. & Croll, D. Genome-wide association mapping reveals genes underlying population-level metabolome diversity in a fungal crop pathogen. BMC Biol. 20, 224 (2022).
- Mukherjee, P. K., Horwitz, B. A. & Kenerley, C. M. Secondary metabolism in Trichoderma – a genomic perspective. Microbiology 158, 35–45 (2012).